Tìm hiểu về kim loại kiềm thổ cũng như cách điều chế | Hải Tiến
Kim loại kiềm thổ và những tính chất vật lý, hóa học của chúng. Cách điều chế các kim loại này cũng như tính ứng dụng trong đời sống
Kim loại kiềm thổ là gì, có những tính chất hóa học và vật lý như thế nào. Đây chắc chắn là câu hỏi của các bạn học sinh khi mới tiếp cận bộ môn hóa học. Hãy cùng Hải Tiến giúp bạn giải đáp những thắc mắc về kim loại này qua bài viết dưới đây nhé.
Mục lục bài viết
Kim loại kiềm thổ là gì
Kim loại kiềm thổ là một dãy những nguyên tố trong nhóm nguyên tố IIA trong bảng tuần hoàn các nguyên tố hóa học. Cụ thể, kiềm thổ đứng trước ngay sau các kim loại kiềm. Điển hình của kim loại này phải kể đến những nguyên tố sau: Magie (Mg), Canxi (Ca), Berili (Be), Strontium (Sr), Bari (Ba), Radium (Ra). Tên của những nguyên tố này đều được đặt tên theo các oxit của nó. Với các đất kiềm, có cách gọi cũ như vôi sống, berilia, magiêsia, baryta và strontiva.
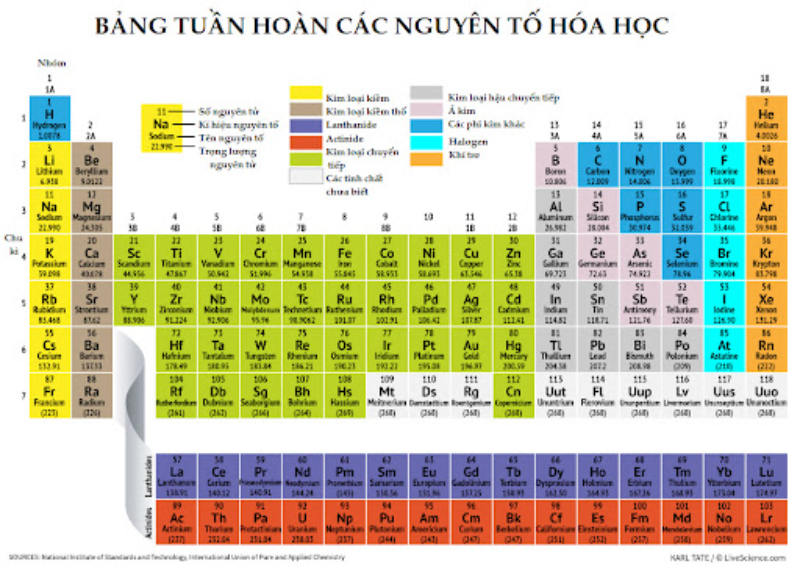
Kim loại kiềm thổ trong bảng tuần hoàn hóa học
Những kim loại này có tên gọi là kiềm thổ bởi những tính chất trong tự nhiên trung gian của nó giữa các chất kiềm (còn có tên gọi là oxit của các kim loại kiềm) và các loại đất hiếm (còn có tên gọi là oxit của các kim loại đất hiếm).
Tính chất vật lý của các kim loại kiềm thổ
Về màu sắc, kim loại kiềm thổ có màu xám nhạt hoặc trắng bạc. Nhiệt độ nóng chảy cũng như nhiệt độ sôi của các kim loại nhóm này tương đối thấp. Độ cứng của chúng thấp và chỉ cứng hơn kim loại kiềm. Khối lượng riêng cũng rất nhỏ bởi trừ Bari thì đây là những kim loại nhẹ hơn nhôm.

Kim loại kiềm thổ có màu xám nhạt hoặc trắng bạc
Ngoại trừ 2 nguyên tố Magie và Berili, các kim loại kiềm thổ tự do và hợp chất đều dễ bay hơi. Chúng sẽ cháy khi có ngọn lửa không màu tác dụng vào khiến cho ngọn lửa có màu đặc trưng. Ví dụ như khi Ca tác dụng với lửa cho màu đỏ da cam, Sr cho màu đỏ son, Ba thì màu lục hơi vàng.
Một số tính chất hóa học của các kim loại kiềm thổ
Các kim loại kiềm thổ có tính khử mạnh chỉ sau các kim loại kiềm. Tính khử của các kim loại này giảm dần từ Ba đến Be
Các kim loại kiềm thổ khi tác dụng với phi kim
Khi các kim loại kiềm được đốt nóng trong không khí thì đều bốc cháy để tạo oxit, phản ứng tỏa ra nhiều nhiệt. Trong không khí ẩm, các nguyên tố Ca, Ba, Sr tạo nên một lớp có tên gọi là Cacbonat cho nên cần lưu trữ các kim loại này trong môi trường bình kín hoặc dầu hỏa khan. Ngoài ra, khi được đun nóng, tất cả các kim loại kiềm thổ đều tác dụng mãnh liệt với nito, lưu huỳnh, phốt pho, halogen, cacbon, silic.

Phản ứng đốt nóng các kim loại kiềm tỏa nhiệt mạnh
Kim loại kiềm thổ khi tác dụng với axit
Khi tác dụng với axit clorua (HCl) hay axit sunfuric (H2SO4), kim loại kiềm khử H+ thành H2. Ví dụ phương trình hóa học:
Ca + 2H+ → Ca2+ + H2
Khi các kim loại này tác dụng với HNO3 hay H2SO4 đặc thì khử N5+ và S6+ thành các hợp chất với mức oxi hóa thấp hơn. Ví dụ:

Kim loại kiềm thổ khi tác dụng với nước
Các kim loại như Ca, Ba, Sr khi tác dụng với nước tạo ra dung dịch bazơ. Trong khi đó, kim loại Mg không tan trong nước lạnh mà chỉ tan trong nước nóng tạo thành Magie oxit (MgO). Và vì có lớp bảo vệ oxit bền mà Be không tan trong nước dù là nước nóng. Tuy nhiên, Be có thể tan trong các dung dịch kiềm mạnh hoặc kiềm nóng chảy tạo ra Berilat.
Những ứng dụng cũng như cách điều chế kim loại kiềm thổ
Trong khi kim loại Be thường được sử dụng làm chất phụ gia để tạo ra các hợp kim có tính đàn hồi cao, bền và chắc; Ca được dùng để tách oxi hay lưu huỳnh ra khỏi thép hoặc làm khô một số hợp chất hữu cơ thì Mg lại là kim loại có ứng dụng nhiều hơn cả. Cụ thể hơn, Mg tạo nên các hợp kim có tính nhẹ, cứng và bền, dùng trong chế tạo tên lửa, máy bay… Ngoài ra, Mg còn được dùng để tổng hợp các chất hữu cơ. Dùng bột Mg trộn với oxi có thể tạo ra chất chiếu sáng ban đêm dùng cho máy ảnh, pháo sáng.

Magie dùng để chế tạo vỏ tên lửa
Điểm đặc biệt của kim loại kiềm thổ chính là chúng chỉ tồn tại ở dạng ion M2+ trong các hợp chất ở ngoài tự nhiên. Chính vì vậy một trong những cách phổ biến điều chế được chúng là điện phân nóng chảy các kim loại này để ra kim loại và khí Clo. Một số phương pháp khác cũng được sử dụng như: Dùng than cốc để khử Magie oxit, canxi oxit từ đolomit trong chân không và tại nhiệt độ cao; hoặc dùng Magie, nhôm khử muối của các loại Canxi, Ba, Sr trong chân không ở nhiệt độ cao từ 1100 độ – 1200 độ C.
Trên đây những chia sẻ kiến thức của Hải Tiến về kim loại kiềm thổ. Hy vọng các bạn sẽ có những giờ học bổ ích và có thể vận dụng những điều trên để hoàn thành bài tập của mình